Manual de Nutrición y Dietética Ángeles Carbajal Azcona. Departamento de Nutrición. Facultad de Farmacia. Universidad Complutense de Madrid https://www.ucm.es/nutricioncarbajal/ 1 7. Hidratos de carbono Hidratos de carbono Recomendaciones dietéticas Sustancias edulcorantes Hidratos de carbono Los hidratos de carbono, carbohidratos (CHO), glúcidos (Glícidos: anglicismo) o azúcares tienen también como función primordial aportar energía, aunque con un rendimiento 2.5 veces menor que el de la grasa. Químicamente, están compuestos por carbono, hidrógeno y oxígeno (Cn:H2n:On). La unidad básica son los monosacáridos (o azúcares simples) de los que glucosa, fructosa y galactosa son nutricionalmente los más importantes. Entre los disacáridos ‐formados por dos monosacáridos‐ destacan sacarosa (glucosa + fructosa), lactosa (el azúcar de la leche: glucosa + galactosa) y maltosa (glucosa + glucosa). Los polisacáridos o hidratos de carbono complejos son moléculas largas compuestas por un número variable de unidades de glucosa unidas entre sí. Nutricionalmente hay que distinguir dos grandes grupos: Almidón, polímero de glucosa formando cadenas lineales o ramificadas (amilosa y amilopectina, respectivamente). Es la forma de almacenamiento de glucosa (de energía) de las plantas. Cuando comemos alimentos de origen vegetal, el almidón es hidrolizado liberando las moléculas de glucosa que nuestro cuerpo utiliza para obtener energía. El glucógeno, un polímero de glucosa con la misma estructura que la amilopectina, sintetizado a partir de glucosa por el hombre y los animales y no por las plantas, se almacena en pequeñas cantidades en el músculo y en el hígado, como reserva energética. No es un componente significativo en la dieta puesto que, tras la muerte del animal, se degrada nuevamente a glucosa. Diversos polisacáridos que reciben el nombre de polisacáridos no amiláceos (no glucémicos) que no son digeridos por los enzimas digestivos del hombre y que constituyen la fibra dietética. Manual de Nutrición y Dietética Ángeles Carbajal Azcona. Departamento de Nutrición. Facultad de Farmacia. Universidad Complutense de Madrid https://www.ucm.es/nutricioncarbajal/ 2 El rendimiento energético medio de los hidratos de carbono es de 4 kcal/gramo, con algunas diferencias entre ellos: los monosacáridos proporcionan 3.74 kcal/g; disacáridos 3.95 kcal/g y almidón 4.18 kcal/g. Además de su papel energético, son fundamentales en el metabolismo de los centros nerviosos pues la glucosa proporciona casi toda la energía que utiliza el cerebro diariamente. La glucosa y su forma de almacenamiento, el glucógeno, suministran aproximadamente la mitad de toda la energía que los músculos y otros tejidos del organismo necesitan para llevar a cabo todas sus funciones (la otra mitad la obtienen de la grasa). También confieren sabor y textura a los alimentos y de esta manera contribuyen al placer de comer. Pero la gente no come glucosa y glucógeno directamente; comemos alimentos ricos en hidratos de carbono que nuestro organismo convierte en glucosa, fuente inmediata de energía, y en glucógeno, una de las reservas energéticas. La glucosa tiene una gran importancia nutricional. Es uno de los dos azúcares de los disacáridos y es la unidad básica de los polisacáridos. Uno de éstos, el almidón, es la principal fuente de energía en la dieta; otro, el glucógeno, es una importante forma de almacenamiento de energía en el organismo. Manual de Nutrición y Dietética Ángeles Carbajal Azcona. Departamento de Nutrición. Facultad de Farmacia. Universidad Complutense de Madrid https://www.ucm.es/nutricioncarbajal/ 3 La sacarosa, presente en algunas verduras y frutas, se obtiene de la caña de azúcar y de la remolacha azucarera. El azúcar (blanco y moreno) es esencialmente sacarosa, constituida por la unión de una molécula de glucosa y una de fructosa. La fructosa es el principal azúcar de las frutas, pero también se encuentra en verduras y hortalizas y, especialmente, en la miel. Es el azúcar más dulce. El poder edulcorante de un azúcar se determina en relación con la sacarosa, el azúcar de referencia (a una solución de 30 g/L a 20ºC se le asigna un poder edulcorante = 1). Poder edulcorante Lactosa 0.25 Galactosa 0.30 Sorbitol, manitol 0.50‐0.60 Glucosa 0.70 Sacarosa 1.00 Xilitol 1.00 Fructosa 1.10‐1.30 La lactosa es el azúcar de la leche, es menos dulce y está formada por glucosa y galactosa. El almidón se encuentra principalmente en cereales, patatas y legumbres. Recomendaciones dietéticas Uno de los aspectos menos satisfactorios de las dietas de las sociedades desarrolladas es la importante disminución producida en la ingesta de hidratos de carbono, consecuencia del menor consumo de algunos alimentos de origen vegetal (pan, patatas y leguminosas, principalmente). Se recomienda que la dieta equilibrada y prudente incluya más de un 55% de la energía total consumida en forma de hidratos de carbono, principalmente complejos, pues está claro su papel en el control del peso corporal y, junto con otros componentes de los alimentos de origen vegetal, en la prevención de la enfermedad cardiovascular, de la diabetes, de algunos tipos de cáncer y de algunos trastornos gastrointestinales. Manual de Nutrición y Dietética Ángeles Carbajal Azcona. Departamento de Nutrición. Facultad de Farmacia. Universidad Complutense de Madrid https://www.ucm.es/nutricioncarbajal/ 4 En España la ingesta ha disminuido considerablemente en los últimos años. ENNA: Estudio Nacional de Nutrición y Alimentación: 1964‐1991 (Varela y col., 1995) MAPA: Panel de consumo 2000‐2008 (del Pozo y col., 2012) ENIDE: 2011, 3.000 encuestas, representativa, transversal, >18 años (AESAN, 2012) Se recomienda igualmente que el aporte calórico de los azúcares sencillos sea inferior al 10% de la energía total consumida. El consumo moderado de azúcares no supone ningún riesgo para la salud y es fuente de placer, aumentando la palatabilidad de la dieta. Sin embargo, en exceso, pueden tener dos efectos poco beneficiosos. Por un lado, pueden contribuir a reducir la concentración de nutrientes de la dieta y aumentar la probabilidad de deficiencias nutricionales pues pueden considerarse como una fuente de calorías vacías. En segundo lugar, un consumo excesivo, junto con otros factores, puede aumentar el riesgo de caries dental. Manual de Nutrición y Dietética Ángeles Carbajal Azcona. Departamento de Nutrición. Facultad de Farmacia. Universidad Complutense de Madrid https://www.ucm.es/nutricioncarbajal/ 5 Sustancias edulcorantes Los edulcorantes son todas aquellas sustancias capaces de proporcionar sabor dulce a un alimento o preparación culinaria. Además de las comentadas en el apartado de hidratos de carbono, hay otras muchas sustancias que también tienen sabor dulce. Pueden clasificarse de la siguiente manera: Edulcorantes naturales (glucosa, fructosa, galactosa, sacarosa, lactosa, maltosa, miel). Edulcorantes nutritivos, obtenidos a partir de sustancias naturales: derivados del almidón (glucosa o jarabe de glucosa), derivados de la sacarosa (azúcar invertido), azúcares‐alcoholes o polioles (sorbitol, manitol, xilitol, ..), neoazúcares (fructo‐oligosacáridos). Todos suministran Calorías. Edulcorantes intensos: (1) químicos o edulcorantes artificiales (sacarina, aspartamo, acesulfamo, ciclamato, alitamo) y (2) edulcorantes intensos de origen vegetal (glicirriza). Los polioles o azúcares‐alcoholes como el sorbitol (2.6 kcal/g; dulzor relativo con respecto a la sacarosa = 0.6) (E 420), manitol (1.6 kcal/g; dulzor relativo con respecto a la sacarosa = 0.5) (E 421) o xilitol (2.4 kcal/g; dulzor relativo con respecto a la sacarosa = 0.7 – 1) (E 967), se obtienen a partir de glucosa o sacarosa por lo que son sustancias relacionadas con los azúcares que se usan frecuentemente en la elaboración de productos dietéticos para diabéticos, pues se absorben muy lentamente. Otro beneficio importante es que no contribuyen al desarrollo de la caries dental, pues las bacterias cariogénicas no pueden metabolizarlos tan rápidamente como el azúcar; además, apenas modifican el pH. Por ello, se emplean con frecuencia para edulcorar chicles, caramelos y, en general, productos que pueden permanecer mucho tiempo en la boca. Consumidos en exceso pueden tener un efecto laxante. Los edulcorantes artificiales, como la sacarina (300 – 600 veces más dulce que la sacarosa) (E 954), el acesulfamo‐K (200 veces más dulce) (E 950) o el ciclamato (30 – 40 veces más dulce) (E 952), son sustancias no relacionadas químicamente con los azúcares que no aportan energía, porque no son metabolizados. La sacarina es rápidamente eliminada por la orina y no se acumula. Aspartamo (160 a 220 veces más dulce que la sacarosa) (E 951), constituido por dos aminoácidos (ácido aspártico y fenilalanina) y alitamo (alanina y ácido aspártico; unas 2000 veces más dulce que la sacarosa), tienen, como proteínas, un rendimiento energético de 4 kcal/gramo. Sin embargo, en ambos casos, su valor calórico es insignificante teniendo en cuenta las pequeñísimas cantidades en las que se consumen.
ISOMERIA
miércoles, 16 de marzo de 2022
sábado, 27 de diciembre de 2014
ISOMERIA
Definición de isómero
Se llaman isómeros a aquellas moléculas que poseen la misma fórmula molecular pero diferente estructura. Se clasifican en isómeros estructurales y estereoisómeros.
Isómeros estructurales
Los isómeros estructurales difieren en la forma de unir los átomos y a su vez se clasifican en isómeros de cadena de posición y de función.
Isómeros estructurales
Definición de isómeros
Se llaman isómeros a moléculas que tienen la misma formula molecular pero distinta estructura. Se clasifican en isómeros de cadena, posición y función.
Isómeros de cadena
Definición de isómero
Se llaman isómeros a aquellas moléculas que poseen la misma fórmula molecular pero diferente estructura. Se clasifican en isómeros estructurales y estereoisómeros.
Isómeros estructurales
Los isómeros estructurales difieren en la forma de unir los átomos y a su vez se clasifican en isómeros de cadena de posición y de función.
Isómeros estructurales
Definición de isómeros
Se llaman isómeros a moléculas que tienen la misma formula molecular pero distinta estructura. Se clasifican en isómeros de cadena, posición y función.
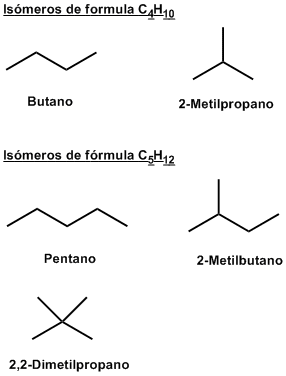
Isómeros de cadena

Se distinguen por la diferente estructura de las cadenas carbonadas. Un ejemplo de este tipo de isómeros son el butano y el 2-metilpropano.
Isómeros de posición
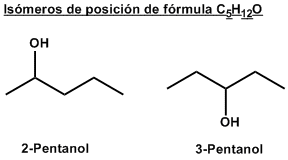
El grupo funcional ocupa una posición diferente en cada isómero. El 2-pentanol y el 3-pentanol son isómeros de posición.
Isómeros de función

El grupo funcional es diferente. El 2-butanol y el dietil éter presentan la misma fórmula molecular, pero pertenecen a familias diferentes -alcohol y éter- por ello se clasifican como isómeros de función.
Isómeros geométricos (cis/trans)
Isomería cis/trans
Son compuestos que difieren en la disposición espacial de sus grupos. Se llaman cis los isómeros geométricos que tienen los grupos al mismo lado y trans los que lo tienen a lados opuestos.
cis y trans-2-Buteno
Isómeros cis y trans del 2-Buteno

Modelos moleculares del cis y trans-2-buteno.

is y trans-1,2-Dimetilciclopentano
Isómeros cis y trans del 1,2-Dimetilciclopentano
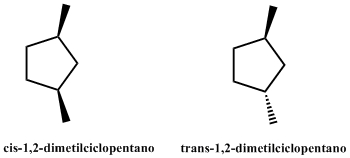
Modelos moleculares del cis y trans-1,2-Dimetilciclopentano.

Estereoisómeros
Los estereoisómeros tienen todos los enlaces idénticos y se diferencian por la disposición espacial de los grupos. Se clasifican en isómeros cis - trans o geométricos, enantiómeros y diastereoisómeros.
Diastereroisómeros
Definición de Diastereoisómeros
Son moléculas que se diferencian por la disposición espacial de los grupos, pero que no son imágenes especulares. Un tipo de diastereoisómeros son los isómeros geométricos (alquenos cis y trans). Para que dos moléculas sean diastereoisómeros es necesario que al menos tengan dos centros quirales. En uno de los centros los sustituyentes están dispuestos igual en ambas moléculas y en el otro deben cambiar.
de diastereoisómeros


Centro quiral o asimétrico
Se llama centro quiral o asimétrico a un átomo unido a cuatro sustituyentes diferentes. Una molécula que posee un centro quiral tiene una imagen especular no superponible con ella, denominada enantiómero.
Enantiómeros
Definición de Enantiómeros
Los enantiómeros son imágenes especulares no superponibles. Se caracterizan por poseer un átomo unido a cuatro grupos distintos llamado asimétrico o quiral.
Nomenclatura de enantiómeros
Reglas para nombrar enantiómeros
Para dar notación R/S a un centro quiral es necesario asignar prioridades a los sustituyentes mediante las siguientes reglas:
Regla 1
Las prioridades de los átomos unidos al quiral se dan por números atómicos. En el caso de isótopos, tiene prioridad el de mayor masa atómica.

Las prioridades se dan por orden de número atómico de los átomos unidos directamente al carbono asimétrico (dibujados en rojo)
Regla 2
Cuando dos o más sustituyentes unidos al centro quiral tengan la misma prioridad, se continua comparando las cadenas átomo a átomo hasta encontrar un punto de diferencia.
Regla 3

Los enlaces dobles y triples se desdoblan considerándolos como si fueran enlaces sencillos.

Para asignar notación R/S seguimos el orden de prioridades a, b, c de los sustituyentes. Si esta sucesión se realiza en el sentido de las agujas del reloj se dice que el centro es R (rectus, latín derecha). Si se sigue el sentido contrario a las agujas al recorrer las prioridades a, b, c se dice que es S (sinester, latín izquierda). Esta regla sólo es válida cuando el grupo d está hacia el fondo del plano (enlace a trazos), si d sale hacia nosotros (cuña) la notación es la contraria (R giro a la izquierda, S giro a la derecha).

Ejemplo de enantiómeros: (R) y (S)-1-Bromo-1-cloroetano
En los modelos moleculares puede verse que las dos moléculas son distintas, no se superponen.


La presencia de un carbono asimétrico (con sustituyentes distintos: metilo, hidrógeno, cloro y bromo)
hace posible que la molécula y su imagen especular sean distintas.
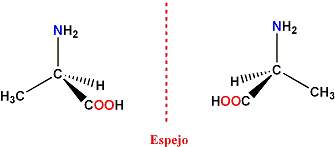
Ejemplo de enantiómeros: (R) y (S)-Alanina
La (R) y (S)-Alanina son otro ejemplo de enantiómeros

Moléculas con varios centros quirales
Máximo número de estereoisómeos
El número máximo de estereoisómeros que presenta una molécula puede calcularse con la fórmula (2n), donde n representa el número de carbonos asimétricos. Así una molécula con 2 centros quirales presenta 4 estereoisómeros.
Estereoisómeros de 2-Bromo-3-clorobutano

Estereoisómeros de 1,2-Dimetilciclohexano

Actividad óptica
Los enantiómeros poseen casi todas las propiedades físicas idénticas, con la excepción de la actividad óptica. Uno de los enantiómeros produce rotación de la luz polarizada a la derecha (dextrógiro) y el otro rota la luz polarizada a la izquierda (levógiro).
Actividad Óptica
Los enantiómeros y la actividad óptica
Los enantiómeros presentan propiedades físicas idénticas, con la excepción de su comportamiento frente a la luz polarizada. Un enantiómero gira el plano de la luz polarizada en el sentido de las agujas del reloj, es dextrógiro (+). El otro enantiómero provoca rotación en el sentido contrario al de las agujas del reloj, es levógiro (-). Este fenómeno asociado a sustancias quirales se conoce como actividad óptica.
Medida de la rotación de la luz
La rotación óptica se mide con un polarímetro que consta de de una fuente de luz, un polarizador del que sale luz oscilando en un único plano, la cubeta que contiene el enantiómero y un analizador que permite medir la rotación de la luz.

VERIFICA TU APRENDIZAJE
Suscribirse a:
Comentarios (Atom)